Link ad
Followers
Sunday, January 2, 2022
Nernst Equation for a Daniell cell
- Nernst gave a relationship between electrode potentials and the concentration of electrolyte solutions known as Nernst equation.
- Reduction Potential under Non-standard Conditions is determined using Nernst Equation when Concentrations is not-equal to 1M. Thus For the cell,
For Daniel cell,
Zn(s)+Cu2+(aq) 🠊 Zn2+(aq) + Cu(s)
Zn(s)|Zn2+(aq)||Cu2+(aq)|Cu
In Daniell cell, the electrode potential for any given concentration of Cu2+ and Zn2+ ions, we write
For Cathode:
E(Cu2+/Cu) = E0(Cu2+/Cu) – RT/2F ln(1/[Cu2+(aq)]
For Anode:
E(Zn2+/Zn) = E0(Zn2+/Zn) – RT/2F ln(1/[Zn2+(aq)]
The cell potential, Ecell = E(Cu2+/Cu) - E(Zn2+/Zn)
= E0(Cu2+/Cu) – RT/2F ln(1/[Cu2+(aq)] - E0(Zn2+/Zn) + RT/2F ln(1/[Zn2+(aq)]
= E0(Cu2+/Cu) -E0(Zn2+/Zn)- RT/2F ln(1/[Cu2+(aq)] + RT/2F ln(1/[Zn2+(aq)]
= E0(Cu2+/Cu) -E0(Zn2+/Zn)- RT/2F (ln(1/[Cu2+(aq)]- ln(1/[Zn2+(aq)])
Therefore, Nernst equation for Daniel cell is
Ecell = E0cell - RT/2F ln [Zn2+]/[Cu2+]
Ecell = E0cell − 2.303RT/2F ln [Zn2+]/[Cu2+]
by putting the value of R= 8.314J/KM ,T=298K, ln=2.303log and F=96457C
Ecell =E0cell − 0.059/2 log[Zn2+]/[Cu2+]
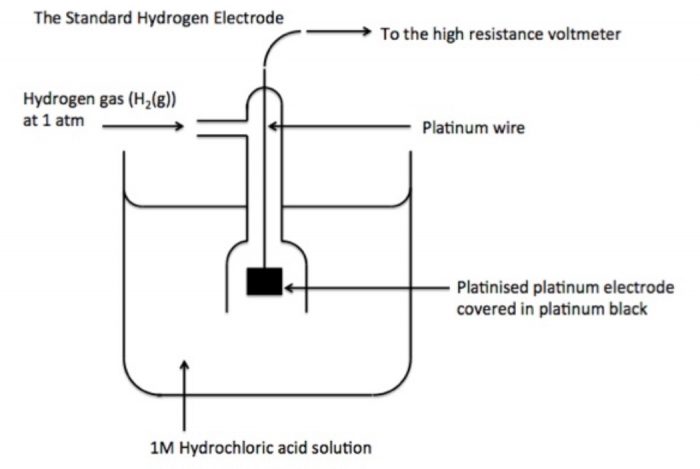
STANDARD HYDROGEN ELECTRODE (SHE)
ü It is reference electrode consists of a platinum electrode(Pt wire fitted in glass tube) in contact with H2 gas (1 atm) and aqueous H+ ions (1 M).
ü It is assigned 0.0 V electrode potential.
ü It may behave as anodic or cathodic half cell.
ü It is represented as
Pt(s)|H2(g)(aH2= 1)|H+(aq)(aH+ = 1).
ü When SHE is coupled with an other half cell then cell potential is the value of the electrode potential of half cell.
EMF and Electrode Potential
EMF: (electromotive force): It is the electrode potential difference across the terminals of the cell when no current is drawn through the cell.
Electrode potential. It is the potential difference develops between the electrode and the electrolyte.
Standard electrode potential : When the concentrations of all the species involved in a half-cell is unity then the electrode potential is known as standard electrode potential.Electrode potential
- More positive: Stronger oxidizing agent and more readily accepts electrons.
- More negative: Stronger reducing agent and more readily gives electrons.
- By combining two half cell reaction, we get a complete net reaction.
- The total cell potential (Ecell) is given by:
Ecell = Ecathode – Eanode
=Eright – E left
Saturday, January 1, 2022
Chemistry Practical Viva Part-1
1. What is the principle of volumetric analysis?
Answer. In volumetric analysis, the concentration of a solution is determined by allowing a known volume of the solution to react, quantitatively with another solution of known concentration.
2. What is titration ?
Answer. The process of adding one solution from the burette to another in the conical flask in order to complete the chemical reaction involved, is known as titration.
3. What is a standard solution ?
Answer. A solution whose strength is known is called a standard solution. 4. What is a normal solution ?
Answer. A solution containing one gram-equivalent mass of the solute per litre of the solution is called a normal solution.
5. What is indicator ?
Answer. Indicator is a chemical substance which changes colour at the end point
6. What is end point ?
Answer. The stage during titration at which the reaction is just complete is known as the end point of titration.
7. Why a titration flask should not be rinsed ? Answer. This is because during rinsing-some liquid will remain sticking to the titration flask therefore the pipetted volume taken in the titration flask will increase.
8. What are primary and secondary standard substances?
Answer. A substance is known as primary standard if it is available in high degree of purity, if it is stable and unaffected by air, if it does not gain or lose moisture in air, if it is readily soluble and its solution in water remains as such for long time. On the other hand, a substance which does not possess the above characteristics is called a secondary standard substance. Primary standards are crystalline oxalic add, anhydrous Na2CO3 , Mohr’s salt, etc.
9. Burette and pipette must be rinsed with the solution with which they are filled, why ?
Answer. The burette and pipette are rinsed with the solution with which they are filled in order to remove any water sticking to their sides, which otherwise would decrease the cone, of the solutions to be taken in them
10.It is customary to read lower meniscus in case of colourless and transparent solutions and upper meniscus in case of highly coloured solutions, why ?
Answer. Because it is easy to read the lower meniscus in case of colourless solutions, while the upper meniscus in case of coloured solutions. In case of coloured solutions lower meniscus is not visible clearly.
11.What is a molar solution ?
Answer. A molar solution is a solution, a litre of which contains one gm-mole of the substance. This is symbolised as 1M.
12.Why the last drop of solution must not be blown out of a pipette?
Answer. Since the drops left in the jet end is extra of the volume measured by the pipette.
13.Pipette should never be held from its bulb, why ?
Answer. The body temperature may expand the glass and introduce an error in the measurement volume.
14. What is permanganometry ?
Answer. Redox titrations involving KMnO4 as the oxidising agent are called permanganometric titrations.
15.Which is an oxidising agent and a reducing agent in the reaction between KMnO4 and FeSO4?
Answer. KMnO4 acts as oxidising agent and FeSO4 acts as reducing agent.
16.What is the indicator used in KMnO4 titration ?
Answer. No indicator is used because KMnO4 acts as a self-indicator
17.Why does KMnO4 act itself as an indicator ?
Answer. In the presence of dilute sulphuric acid, KMnO4 reacts with reducing agent (oxalic acid or . ferrous sulphate). When all the reducing agent has been oxidised, the excess of KMnO4 is not decomposed and imparts pink colour to the solution.
18.What is the end point in KMnO4 titrations ? Answer. From colourless to permanent light pink.
19.Why is Mohr’s salt preferred as a primary standard over ferrous sulphate in volumetric analysis ?
Answer. This is because of the fact that Mohr’s salt is stable and is not readily oxidised by air. Ferrous sulphate gets oxidised to ferric sulphate.
20. Why are a few drops of dilute sulphuric acid added while preparing a standard solution of Mohr’s salt ?
Answer. Few drops of H2SO4 are added to prevent the hydrolysis of ferrous sulphate.
21.Why a burette with rubber pinch cock should not be used in KMnO4 titrations ? Answer. Because KMnO4 attacks rubber.
22.Sometimes a brown ppt. is observed in KMnO4 titrations. Why ?
Answer. It is due to insufficient quantity of dil. sulphuric acid. Brown coloured ppt. (MnO2.H20) is formed due to the incomplete oxidation of KMnO4.
23.Why should you heat the oxalic acid solution to about 60-70°C before titrating with KMnO4 solution ?
Answer. In cold, the reaction is very slow due to the slow formation of Mn 2+ ions. Oxalic acid is heated to speed up the liberation of Mn 2+ ions which then autocatalyses the reaction and thus the reaction proceeds rapidly. This also serves the purpose of expelling the carbondioxide evolved during the reaction which otherwise does not allow the reaction to go to completion.
24.What is the equivalent mass of KMnO4 when it acts as oxidizing agent in acidic medium ?
Answer. KMnO4 loses 5 electrons per molecule, when it acts as oxidizing agent in the presence of acids. Therefore, its equivalent mass is one-fifth of its molecular mass.
25.Are ‘molality’ and “molarity’’ same ?
Answer. No, molality of a solution is defined as the number of moles of solute present in 1000 grams of the solution whereas molarity tells us about the number of moles of the solute present per litre of the solution.
26.What is the basicity of H2SO4 ?
Answer. 2.
The History of New Year Celebration
नव वर्ष एक उत्सव की तरह पूरे विश्व में अलग-अलग स्थानों पर अलग-अलग तिथियों तथा विधियों से मनाया जाता है। विभिन्न सम्प्रदायों के नव वर्ष समारोह भिन्न-भिन्न होते हैं और इसके महत्त्व की भी विभिन्न संस्कृतियों में परस्पर भिन्नता है।
पश्चिमी नव वर्ष
नव वर्ष उत्सव 4,000 वर्ष पहले से बेबीलोन में मनाया जाता था। लेकिन उस समय नए वर्ष का ये त्यौहार 21 मार्च को मनाया जाता था जो कि वसंत के आगमन की तिथि भी मानी जाती थी। प्राचीन रोम में भी नव वर्षोत्सव के लिए चुनी गई थी। रोम के शासक जूलियस सीजर ने ईसा पूर्व 45वें वर्ष में जब जूलियन कैलेंडर की स्थापना की, उस समय विश्व में पहली बार 1 जनवरी को नए वर्ष का उत्सव मनाया गया। ऐसा करने के लिए जूलियस सीजर को पिछला वर्ष, यानि, ईसापूर्व 46 इस्वी को 445 दिनों का करना पड़ा था।
हिब्रू नव वर्ष
हिब्रू मान्यताओं के अनुसार भगवान द्वारा विश्व को बनाने में सात दिन लगे थे। इस सात दिन के संधान के बाद नया वर्ष मनाया जाता है। यह दिन ग्रेगरी के कैलेंडर के मुताबिक ५ सितम्बर से ५ अक्टूबर के बीच आता है।
हिन्दुओं का नया साल
हिन्दुओं का नया साल चैत्र नव रात्रि के प्रथम दिन यानी गुड़ी पड़वा पर हर साल विक्रम संवत के अनुसार चैत्र शुक्ल प्रतिपदा से आरंभ होता है।
भारतीय नववर्ष
भारत के विभिन्न हिस्सों में नव वर्ष अलग-अलग तिथियों को मनाया जाता है। प्रायः ये तिथि मार्च और अप्रैल के महीने में पड़ती है। पंजाब में नया साल बैशाखी नाम से १३ अप्रैल को मनाई जाती है। सिख नानकशाही कैलंडर के अनुसार १४ मार्च होला मोहल्ला नया साल होता है। इसी तिथि के आसपास बंगाली तथा तमिळ नव वर्ष भी आता है। तेलगु नया साल मार्च-अप्रैल के बीच आता है। आंध्रप्रदेश में इसे उगादी (युगादि=युग+आदि का अपभ्रंश) के रूप में मनाते हैं। यह चैत्र महीने का पहला दिन होता है। तमिल नया साल विशु १३ या १४ अप्रैल को तमिलनाडु और केरल में मनाया जाता है। तमिलनाडु में पोंगल १५ जनवरी को नए साल के रूप में आधिकारिक तौर पर भी मनाया जाता है। कश्मीरी कैलेंडर नवरेह १९ मार्च को होता है। महाराष्ट्र में गुड़ी पड़वा के रूप में मार्च-अप्रैल के महीने में मनाया जाता है, कन्नड नया वर्ष उगाडी कर्नाटक के लोग चैत्र माह के पहले दिन को मनाते हैं, सिंधी उत्सव चेटी चंड, उगाड़ी और गुड़ी पड़वा एक ही दिन मनाया जाता है। मदुरै में चित्रैय महीने में चित्रैय तिरूविजा नए साल के रूप में मनाया जाता है। मारवाड़ी नया साल दीपावली के दिन होता है। गुजराती नया साल दीपावली के दूसरे दिन होता है। इस दिन जैन धर्म का नववर्ष भी होता है।लेकिन यह व्यापक नहीं है। अक्टूबर या नवंबर में आती है। बंगाली नया साल पोहेला बैसाखी १४ या १५ अप्रैल को आता है। पश्चिम बंगाल और बांग्लादेश में इसी दिन नया साल होता है।
चैत्र शुक्ल प्रतिपदा का ऐतिहासिक महत्व :
1) इसी दिन के सूर्योदय से ब्रह्माजी ने सृष्टि की रचना प्रारंभ की।
2) सम्राट विक्रमादित्य ने इसी दिन राज्य स्थापित किया। इन्हीं के नाम पर विक्रमी संवत् का पहला दिन प्रारंभ होता है।
3) प्रभु श्री राम के राज्याभिषेक का दिन यही है।
4) शक्ति और भक्ति के नौ दिन अर्थात् नवरात्र का पहला दिन यही है।
5) सिखो के द्वितीय गुरू श्री अंगद देव जी का जन्म दिवस है।
6) स्वामी दयानंद सरस्वती जी ने इसी दिन आर्य समाज की स्थापना की एवं कृणवंतो विश्वमआर्यम का संदेश दिया।
7) सिंध प्रान्त के प्रसिद्ध समाज रक्षक वरूणावतार भगवान झूलेलाल इसी दिन प्रगट हुए।
8) राजा विक्रमादित्य की भांति शालिवाहन ने हूणों को परास्त कर दक्षिण भारत में श्रेष्ठतम राज्य स्थापित करने हेतु यही दिन चुना। विक्रम संवत की स्थापना की ।
9) युधिष्ठिर का राज्यभिषेक भी इसी दिन हुआ।
10) संघ संस्थापक प.पू.डॉ. केशवराव बलिराम हेडगेवार का जन्म दिन।
11) महर्षि गौतम जयंती
भारतीय नववर्ष का प्राकृतिक महत्व :
1) वसंत ऋतु का आरंभ वर्ष प्रतिपदा से ही होता है जो उल्लास, उमंग, खुशी तथा चारों तरफ पुष्पों की सुगंधि से भरी होती है।
2) फसल पकने का प्रारंभ यानि किसान की मेहनत का फल मिलने का भी यही समय होता है।
3) नक्षत्र शुभ स्थिति में होते हैं अर्थात् किसी भी कार्य को प्रारंभ करने के लिये यह शुभ मुहूर्त होता है।
भारतीय नववर्ष कैसे मनाएँ :
1) हम परस्पर एक दुसरे को नववर्ष की शुभकामनाएँ दें। पत्रक बांटें , झंडे, बैनर....आदि लगावे ।
2) आपने परिचित मित्रों, रिश्तेदारों को नववर्ष के शुभ संदेश भेजें।
3) इस मांगलिक अवसर पर अपने-अपने घरों पर भगवा पताका फेहराएँ।
4) आपने घरों के द्वार, आम के पत्तों की वंदनवार से सजाएँ।
5) घरों एवं धार्मिक स्थलों की सफाई कर रंगोली तथा फूलों से सजाएँ।
6) इस अवसर पर होने वाले धार्मिक एवं सांस्कृतिक कार्यक्रमों में भाग लें अथवा कार्यक्रमों का आयोजन करें।
7) प्रतिष्ठानों की सज्जा एवं प्रतियोगिता करें। झंडी और फरियों से सज्जा करें।
8) इस दिन के महत्वपूर्ण देवताओं, महापुरुषों से सम्बंधित प्रश्न मंच के आयोजन करें।
9) वाहन रैली, कलश यात्रा, विशाल शोभा यात्राएं कवि सम्मेलन, भजन संध्या , महाआरती आदि का आयोजन करें।
10) चिकित्सालय, गौशाला में सेवा, रक्तदान जैसे कार्यक्रम।
इस्लामिक कैलेंडर का नया साल
इस्लामिक कैलेंडर का नया साल मुहर्रम होता है। इस्लामी कैलेंडर एक पूर्णतया चन्द्र आधारित कैलेंडर है जिसके कारण इसके बारह मासों का चक्र ३३ वर्षों में सौर कैलेंडर को एक बार घूम लेता है। इसके कारण नव वर्ष प्रचलित ग्रेगरी कैलेंडर में अलग अलग महीनों में पड़ता है।
If you know more about new year celebration in different country , Click Here
feature post
CARBON AND ITS COMPOUNDS-Functional Group
1. Name the functional groups present in the following compounds. a) CH 3 – CO –CH 2 –CH 2 –CH 2 –CH 3 b) CH...